De warmtecapaciteit van een gas is de hoeveelheid energie die een lichaam absorbeert wanneer het met één graad wordt verwarmd. Laten we de belangrijkste kenmerken van deze fysieke hoeveelheid analyseren.

Definities
De soortelijke warmte van een gas is de eenheidsmassa van een bepaalde stof. De meeteenheden zijn J/(kg·K). De hoeveelheid warmte die door het lichaam wordt geabsorbeerd tijdens het veranderen van de aggregatietoestand, wordt niet alleen geassocieerd met de begin- en eindtoestand, maar ook met de overgangsmethode.

Afdeling
De warmtecapaciteit van gassen wordt gedeeld door de waarde bepaald bij constant volume (Cv), constante druk (Cр).
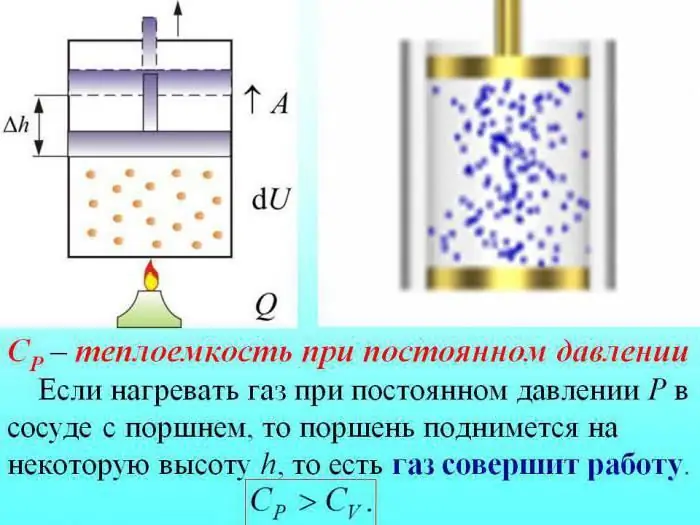
In het geval van verwarming zonder de druk te veranderen, wordt wat warmte verbruikt om het werk van gasexpansie te produceren, en een deel van de energie wordt gebruikt om de interne energie te verhogen.
De warmtecapaciteit van gassen bij constante druk wordt bepaald door de hoeveelheid warmte die wordt besteed aan het verhogen van de interne energie.
Gasstatus: kenmerken, beschrijving
De warmtecapaciteit van een ideaal gas wordt bepaald rekening houdend met het feit dat Сp-Сv=R. Deze laatste grootheid wordt de universele gasconstante genoemd. De waarde komt overeen met 8,314 J/(mol K).
Bij het uitvoeren van theoretische berekeningen van warmtecapaciteit, bijvoorbeeld het beschrijven van de relatie met temperatuur, is het niet voldoende om alleen thermodynamische methoden te gebruiken, het is belangrijk om jezelf te wapenen met elementen van statische fysica.
De warmtecapaciteit van gassen omvat de berekening van de gemiddelde waarde van de energie van de translatiebeweging van sommige moleculen. Een dergelijke beweging wordt samengevat uit de rotatie- en translatiebeweging van het molecuul, evenals uit de interne trillingen van atomen.
In de statische fysica is er informatie dat voor elke graad van vrijheid van rotatie- en translatiebeweging, er een hoeveelheid voor een gas is die gelijk is aan de helft van de universele gasconstante.

Interessante feiten
Een deeltje van een monoatomisch gas wordt verondersteld drie translationele vrijheidsgraden te hebben, dus de soortelijke warmte van een gas heeft drie translationele, twee rotationele en één vibrationele vrijheidsgraden. De wet van hun uniforme verdeling leidt tot het gelijkstellen van de soortelijke warmte bij een constant volume aan R.
Tijdens de experimenten bleek dat de warmtecapaciteit van een diatomisch gas overeenkomt met de waarde R. Een dergelijke discrepantie tussen theorie en praktijk wordt verklaard door het feit dat de warmtecapaciteit van een ideaal gas wordt geassocieerd met kwantum effecten, daarom is het bij het maken van berekeningen belangrijk om statistieken te gebruiken op basis van quantummechanica.
Gebaseerd op de fundamenten van de kwantummechanica, heeft elk systeem van deeltjes die oscilleren of roteren, inclusief gasmoleculen, slechts enkele discrete energiewaarden.
Als de energie van thermische beweging in het systeem niet voldoende is om oscillaties met een bepaalde frequentie op te wekken, dragen dergelijke bewegingen niet bij aan de totale warmtecapaciteit van het systeem.
Als gevolg hiervan wordt een bepaalde mate van vrijheid "bevroren", het is onmogelijk om de wet van equipartitie daarop toe te passen.
De warmtecapaciteit van gassen is een belangrijk kenmerk van de toestand waarvan het functioneren van het gehele thermodynamische systeem afhangt.
De temperatuur waarbij de wet van equipartitie kan worden toegepast op de vibrationele of roterende vrijheidsgraad wordt gekenmerkt door de kwantumtheorie, verbindt de constante van Planck met de Boltzmann-constante.

Diatomische gassen
De openingen tussen de rotatie-energieniveaus van dergelijke gassen zijn een klein aantal graden. De uitzondering is waterstof, waarbij de temperatuurwaarde wordt bepaald door honderden graden.
Daarom is de warmtecapaciteit van een gas bij constante druk moeilijk te beschrijven door de wet van uniforme verdeling. In kwantumstatistieken wordt er bij het bepalen van de warmtecapaciteit rekening mee gehouden dat het trillingsdeel ervan, in het geval van een temperatuurdaling, snel afneemt en nul bereikt.
Dit fenomeen verklaart het feit dat er bij kamertemperatuur praktisch geen vibrerend deel van de warmtecapaciteit is, voordiatomisch gas, het komt overeen met de constante R.
De warmtecapaciteit van een gas bij constant volume in het geval van lage temperatuurindicatoren wordt bepaald met behulp van kwantumstatistieken. Er is het Nernst-principe, dat de derde wet van de thermodynamica wordt genoemd. Op basis van de formulering zal de molaire warmtecapaciteit van een gas afnemen met afnemende temperatuur, tot nul.

Kenmerken van vaste stoffen
Als de warmtecapaciteit van een mengsel van gassen kan worden verklaard met behulp van kwantumstatistieken, dan wordt thermische beweging voor een vaste aggregatietoestand gekenmerkt door kleine fluctuaties van deeltjes nabij de evenwichtspositie.
Elk atoom heeft drie vibrationele vrijheidsgraden, daarom kan, in overeenstemming met de equipartitiewet, de molaire warmtecapaciteit van een vaste stof worden berekend als 3nR, waarbij n het aantal atomen in een molecuul is.
In de praktijk is dit aantal de limiet waartoe de warmtecapaciteit van een vast lichaam bij hoge temperaturen neigt.
Maximum kan worden verkregen bij gewone temperaturen voor sommige elementen, waaronder metalen. Voor n=1 is voldaan aan de wet van Dulong en Petit, maar voor complexe stoffen is het nogal moeilijk om een dergelijke limiet te bereiken. Aangezien de limiet in werkelijkheid niet kan worden bereikt, vindt ontleding of smelten van de vaste stof plaats.
Geschiedenis van de kwantumtheorie
De grondleggers van de kwantumtheorie zijn Einstein en Debye aan het begin van de twintigste eeuw. Het is gebaseerd op de kwantisering van oscillerende bewegingen van atomen in een bepaaldekristal. In het geval van lage temperatuurindicatoren blijkt de warmtecapaciteit van een vast lichaam recht evenredig te zijn met de absolute waarde in blokjes. Deze relatie wordt de wet van Debye genoemd. Als criterium dat het mogelijk maakt onderscheid te maken tussen lage en hoge temperatuurindicatoren, wordt hun vergelijking met de Debye-temperatuur genomen.
Deze waarde wordt bepaald door het spectrum van trillingen van een atoom in het lichaam, daarom hangt het sterk af van de kenmerken van zijn kristalstructuur.
QD is een waarde die enkele honderden K heeft, maar bijvoorbeeld veel hoger is in diamant.
De geleidingselektronen leveren een belangrijke bijdrage aan de warmtecapaciteit van metalen. Om het te berekenen, worden de Fermi-kwantumstatistieken gebruikt. De elektronische geleidbaarheid van metaalatomen is recht evenredig met de absolute temperatuur. Aangezien het een onbeduidende waarde is, wordt er alleen rekening mee gehouden bij temperaturen die neigen naar het absolute nulpunt.
Methoden voor het bepalen van de warmtecapaciteit
De belangrijkste experimentele methode is calorimetrie. Om een theoretische berekening van de warmtecapaciteit uit te voeren, wordt gebruik gemaakt van statistische thermodynamica. Het is geldig voor een ideaal gas, evenals voor kristallijne lichamen, wordt uitgevoerd op basis van experimentele gegevens over de structuur van materie.
Empirische methoden voor het berekenen van de warmtecapaciteit van een ideaal gas zijn gebaseerd op het idee van de chemische structuur, de bijdrage van individuele groepen atomen aan Ср.
Voor vloeistoffen worden ook methoden gebruikt die gebaseerd zijn op het gebruik van thermodynamicacycli die het mogelijk maken om van de warmtecapaciteit van een ideaal gas naar een vloeistof over te gaan door de afgeleide van de temperatuur van de enthalpie van het verdampingsproces.
In het geval van een oplossing is de berekening van de warmtecapaciteit als een additieve functie niet toegestaan, aangezien de overwaarde van de warmtecapaciteit van de oplossing in wezen significant is.
Om het te evalueren, hebben we de moleculair-statistische theorie van oplossingen nodig. Het moeilijkste is de identificatie van de warmtecapaciteit van heterogene systemen in thermodynamische analyse.

Conclusie
De studie van warmtecapaciteit stelt je in staat om de energiebalans te berekenen van processen die plaatsvinden in chemische reactoren, evenals in andere chemische productie-apparaten. Bovendien is deze waarde nodig voor de selectie van optimale soorten koelvloeistoffen.
Op dit moment is de experimentele bepaling van de warmtecapaciteit van stoffen voor verschillende temperatuurintervallen - van lage waarden tot hoge waarden - de belangrijkste optie voor het bepalen van de thermodynamische eigenschappen van een stof. Bij het berekenen van de entropie en enthalpie van een stof worden warmtecapaciteitsintegralen gebruikt. Met informatie over de warmtecapaciteit van chemische reagentia in een bepaald temperatuurbereik kunt u het thermische effect van het proces berekenen. Informatie over de warmtecapaciteit van oplossingen maakt het mogelijk om hun thermodynamische parameters te berekenen bij elke temperatuurwaarde binnen het geanalyseerde interval.
Een vloeistof wordt bijvoorbeeld gekenmerkt door het verbruik van een deel van de warmte om de waarde van potentiële energie te veranderenreagerende moleculen. Deze waarde wordt de "configuratie" warmtecapaciteit genoemd en wordt gebruikt om oplossingen te beschrijven.
Het is moeilijk om volwaardige wiskundige berekeningen uit te voeren zonder rekening te houden met de thermodynamische eigenschappen van een stof, zijn aggregatietoestand. Daarom wordt voor vloeistoffen, gassen, vaste stoffen een eigenschap als specifieke warmtecapaciteit gebruikt, die het mogelijk maakt om de energieparameters van een stof te karakteriseren.






