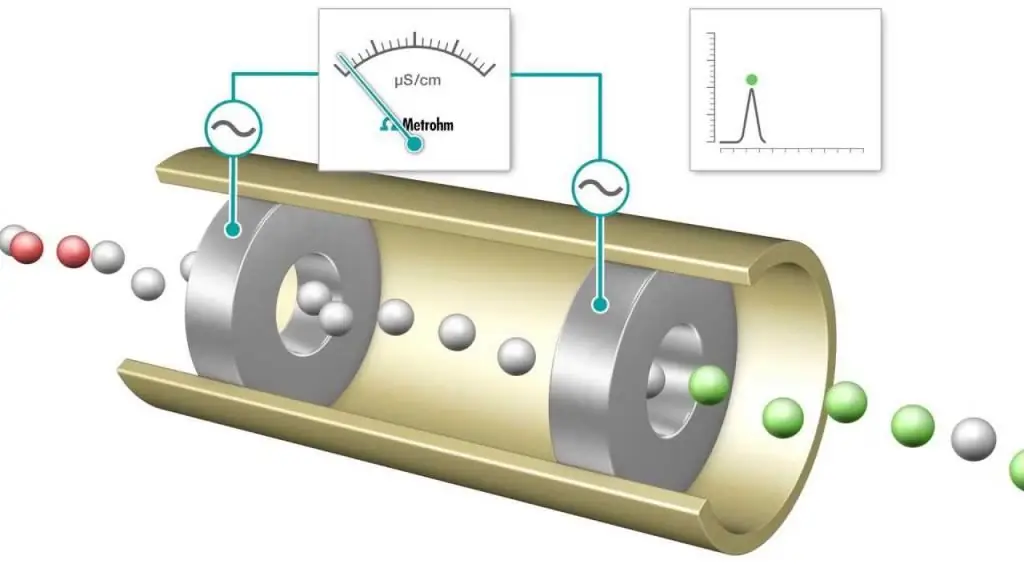
De conductometrische analysemethode is de meting van de elektrolytische geleidbaarheid om de voortgang van een chemische reactie te volgen. Deze wetenschap wordt veel toegepast in de analytische chemie, waar titratie een standaardmethode is. Wat is conductometrie? In de gangbare praktijk in de analytische chemie wordt de term gebruikt als synoniem voor titratie, terwijl het ook wordt gebruikt om niet-titratietoepassingen te beschrijven. Wat is het voordeel van het gebruik van deze analysemethode? Het wordt vaak gebruikt om de algehele geleidbaarheid van een oplossing te bepalen of om het eindpunt van een titratie met ionen te analyseren.
Geschiedenis
Geleidende metingen begonnen al in de 18e eeuw, toen Andreas Baumgartner merkte dat het zoute en mineraalwater van Bad Gastein inOostenrijk geleidt elektriciteit. Zo begon het gebruik van deze methode om de zuiverheid van water te bepalen, die tegenwoordig vaak wordt gebruikt om de effectiviteit van waterzuiveringssystemen te testen, in 1776. Zo begon de geschiedenis van de conductometrische analysemethode.
Friedrich Kohlrausch zette de ontwikkeling van deze wetenschap voort in de jaren 1860, toen hij wisselstroom toepaste op water, zuren en andere oplossingen. Rond deze tijd vond Willis Whitney, die de interacties van zwavelzuur- en chroomsulfaatcomplexen bestudeerde, het eerste conductometrische eindpunt. Deze bevindingen culmineerden in potentiometrische titratie en het eerste instrument voor volumetrische analyse door Robert Behrend in 1883 in de titratie van chloride en bromide HgNO3. De moderne conductometrische analysemethode is dus gebaseerd op Behrend.
Deze ontwikkeling maakte het mogelijk om de oplosbaarheid van zouten en de concentratie van waterstofionen te testen, evenals zuur-base- en redoxtitraties. De conductometrische analysemethode werd verbeterd met de ontwikkeling van de glaselektrode, die in 1909 begon.
Titratie
Conductometrische titratie is een meting waarbij de elektrolytische geleidbaarheid van een reactiemengsel continu wordt gecontroleerd door één reagens toe te voegen. Het equivalentiepunt is het punt waarop de geleidbaarheid plotseling verandert. Een merkbare toename of afname van de geleidbaarheid gaat gepaard met een verandering in de concentratie van de twee meest geleidende ionen, waterstof- en hydroxide-ionen. Deze methodekan worden gebruikt om gekleurde oplossingen of homogene suspensies (bijv. houtpulpsuspensie) te titreren die niet kunnen worden gebruikt met conventionele indicatoren.
Zuur-base- en redoxtitraties worden vaak uitgevoerd, waarbij gemeenschappelijke indicatoren worden gebruikt om het eindpunt te bepalen, zoals methyloranje, fenolftaleïne voor zuur-basetitratie en zetmeeloplossingen voor een jodometrische-type redoxproces. Elektrische geleidbaarheidsmetingen kunnen echter ook worden gebruikt als hulpmiddel om het eindpunt te bepalen, bijvoorbeeld bij het observeren van een oplossing van HCl met de sterke base NaOH.
Protonenneutralisatie
Naarmate de titratie vordert, worden protonen geneutraliseerd om NaOH te vormen door water te vormen. Voor elke toegevoegde hoeveelheid NaOH wordt een equivalent aantal waterstofionen verwijderd. In feite wordt het mobiele H+-kation vervangen door het minder mobiele Na+-ion, en de geleidbaarheid van de getitreerde oplossing, evenals de gemeten celgeleidbaarheid, neemt af. Dit gaat door totdat een equivalentiepunt is bereikt waarbij een oplossing van natriumchloride-NaCl kan worden verkregen. Als er meer base wordt toegevoegd, is er een toename naarmate er meer Na+ en OH- ionen worden toegevoegd en de neutralisatiereactie verwijdert niet langer een aanzienlijke hoeveelheid H+.

Als een sterk zuur getitreerd wordt met een sterke base, heeft de geleidbaarheid dus een minimum op het equivalentiepunt. Dit minimumkan worden gebruikt in plaats van een indicatorkleurstof om het eindpunt van een titratie te bepalen. De titratiecurve is een grafiek van gemeten waarden van geleidbaarheid of geleidbaarheid als functie van het volume toegevoegde NaOH-oplossing. De titratiecurve kan worden gebruikt om het equivalentiepunt grafisch te bepalen. De conductometrische analysemethode (en het gebruik ervan) is uiterst relevant in de moderne chemie.
Reactie
Voor een reactie tussen een zwakke zuur-zwakke base neemt eerst de elektrische geleidbaarheid iets af, aangezien er weinig beschikbare H+ ionen worden gebruikt. Dan neemt de geleidbaarheid iets toe tot het volume van het equivalentiepunt door de bijdrage van het zoutkation en het anion (deze bijdrage in het geval van een sterk zure base is verwaarloosbaar en wordt daar niet meegerekend.) Nadat het equivalentiepunt is bereikt, de geleidbaarheid neemt snel toe door een overmaat aan OH-ionen.
Geleidbaarheidsdetectoren (conductometrische analysemethode) worden ook gebruikt om elektrolytconcentraties in waterige oplossingen te meten. De molaire concentratie van de analyt die de geleidbaarheid van de oplossing creëert, kan worden verkregen uit de gemeten elektrische weerstand van de oplossing.
Conductometrische analysemethode: principe en formules
(2.4.13) C=Constcell1Λm1Res, waarbij Constcell een constante waarde is, afhankelijk van de meetcel, Res is de elektrische weerstand gemeten door het apparaat (volgens de wet van Ohm Res=I / V, en met een constante spanning V-meting I intensiteit stelt u in staat om Res te berekenen), en Λm is het equivalentgeleidbaarheid voor ionische deeltjes. Hoewel Λm voor praktische doeleinden als constant kan worden beschouwd, hangt het af van de concentratie volgens de wet van Kohlrausch:
(2.4.14)=Хт Λm0-ΘC, waarbij Θ een constante is, en Λm0 de beperkende molaire geleidbaarheidskarakteristiek van elk ion is. De molaire geleidbaarheid is op zijn beurt afhankelijk van de temperatuur.
Schrijf
De ontwikkeling van de conductometrische methode voor meetanalyse heeft wetenschappers tot nieuwe ontdekkingen gebracht. De wetenschappers bepaalden de kritische oververzadigingsverhouding, Scrit, met behulp van conductometrie in een homogeen AgCl-precipitatiesysteem met meer dan Ag+-ionen, met behulp van alkylchloridehydrolyse als bron van CI-ionen.” Ze vonden Scrit=1,51, 1,73 en 1,85 bij respectievelijk 15, 25 en 35°C, waarbij S=([Ag+][Cl-] / Ksp) 1/2 volgens hun definitie. Als deze definitie van de oververzadigingsfactor wordt omgezet naar de onze (S=[Ag+][Cl-] / Ksp), zijn de resultaten respectievelijk 2,28, 2,99 en 3,42, wat redelijk goed overeenkomt met de resultaten van de huidige studie. De temperatuurafhankelijkheid van Scrit is echter tegengesteld aan die beschreven in de huidige studie. Hoewel de reden voor deze tegenstrijdigheid niet duidelijk is, kan de afname in Scrit met toenemende temperatuur redelijk redelijk zijn, aangezien de kiemvormingssnelheid dramatisch verandert met een kleine verandering in ΔGm/ kT, en dus ΔGm/ kT, wat evenredig is met T − 3 (lnSm) 2 volgens formule (1.4.12) wordt als bijna constant beschouwd bij temperatuurverandering in het gegeven systeem. Overigens moet de definitie van S [Ag +] [Cl -] / Ksp zijn, aangezien de oververzadigingsverhouding in termen van[AgCl]-monomeerconcentratie wordt aanvankelijk gegeven als S=[AgCl] / [AgCl] (∞)=[Ag +] [Cl -] / Ksp.
Tanaka en Iwasaki
De geschiedenis van de conductometrische analysemethode werd voortgezet door twee iconische Japanse wetenschappers. Tanaka en Iwasaki bestudeerden het proces van nucleatie van AgCl- en AgBr-deeltjes met behulp van de gestopte stroommethode in combinatie met een meerkanaals spectrofotometer, die nuttig is voor het bestuderen van een snel proces in de orde van grootte van msec. Ze ontdekten dat een specifiek zilverhalogenidecomplex AgXm (m-1), met een vrij smalle UV-absorptieband, onmiddellijk werd gevormd wanneer een oplossing van AgC104 in de orde van 10-4 mol dm-3 werd gemengd met een KX (X=Cl of Br) oplossing in de orde van grootte van 10-2 tot 10-1 mol dm-3 gevolgd door een snel verval van ongeveer 10 ms met de vorming van een tussenproduct met een brede UV-absorptie en een veel langzamere verandering in het spectrum van het tussenproduct. Ze interpreteerden het tussenproduct als monodisperse kernen (AgX) n bestaande uit n moleculen en bepaalden n uit de schijnbare verhouding -dC/dt α Cn op t=0 voor verschillende beginconcentraties van C-precursor AgXm (m-1) - (n=7 -10 voor AgCl, n=3-4 voor AgBr).

Echter, aangezien de voorloper AgXm (m − 1) op een niet-stationaire manier verv alt, is de theorie van quasi-stationaire kiemvorming niet van toepassing in dit proces, en dus komt de resulterende waarde van n niet overeen met de nwaarde van kritieke kernen. Als het tussenproduct monodisperse kernen n bevat,gevormd door het monomere complex, kan de -dC/dt α C-verhouding niet worden gehandhaafd. Tenzij we aannemen dat clusters kleiner dan n-meren in evenwicht zijn, ki − 1, ici − 1c1=ki, i − 1ci, met elkaar in een opeenvolgende reactie c1 → c2 → c3 →… → cn − 1 → cn., en alleen de laatste stap cn − 1 → cn is onomkeerbaar; d.w.z. c1⇌c2⇌c3⇌… ⇌cn − 1 → cn.
Bovendien moet worden aangenomen dat de concentraties van clusters van 2 tot n-1 verwaarloosbare evenwichtsconcentraties hebben. Er lijkt echter geen grond te zijn om deze veronderstellingen te rechtvaardigen. Aan de andere kant hebben we geprobeerd de stralen van kritische kernen en de oververzadigingscoëfficiënten S aan het einde van het snelle proces te berekenen, met γ=101 mJ m − 2 voor kubieke AgCl19 en γ=109 mJ m − 2 voor kubieke AgBr20, ervan uitgaande dat de waarden van n, 7-10 voor AgCl19 en 3-4 voor AgBr20, gelijk zijn aan de grootte van monodisperse kernen, n. De conductometrische analysemethode, waarvan de beoordelingen variëren van eenvoudig goedkeuren tot bewonderen, gaf een nieuwe geboorte aan de chemie als wetenschap.
Als resultaat ontdekten wetenschappers de volgende formule: r=0,451 nm en S=105 voor AgCl met n=9; r=0,358 nm en S=1230 voor AgBr met n=4. Omdat hun systemen vergelijkbaar zijn met die van Davis en Jones, die een kritische oververzadiging van AgCl van ongeveer 1,7-2,0 bij 25 °C verkregen. Met behulp van direct-mix conductometrie in gelijke volumes verdunde waterige oplossingen van AgNO3 en KCl, kunnen extreem hoge S-waarden mogelijk niet de werkelijke oververzadigingsfactoren weerspiegelen.in evenwicht met tussenliggende kernen.
UV-absorptie
Het lijkt redelijker om een tussenproduct met brede UV-absorptie toe te schrijven aan veel grotere dan gemiddelde kernen met een brede grootteverdeling die wordt gegenereerd door een niet-stationaire opeenvolgende reactie. De daaropvolgende langzame verandering van tussenliggende kernen lijkt verband te houden met hun rijping in Ostwald.

In de bovenstaande context heeft de Amerikaanse chemicus Nielsen ook een vergelijkbare nrond 12 en een overeenkomstige S groter dan 103 afgeleid voor de kiemvorming van bariumsulfaatdeeltjes uit troebelheidsmetingen als een functie van oververzadiging, met behulp van n=dlogJ / dlogC in een Becher-Dering-achtige theorie aan de formule. (1.3.37), maar gevend (n+ 1) in plaats van n. Aangezien oplossingen van bariumionen en sulfaationen in dit experiment direct werden gemengd, zou de snelle voorbijgaande nucleatie onmiddellijk na het mengen moeten zijn beëindigd, en wat werd gemeten zou de snelheid kunnen zijn van de langzame daaropvolgende Ostwald-rijping en/of fusie van de gegenereerde kernen. Blijkbaar is dit de reden voor de onredelijk lage waarde van n en de extreem hoge oververzadiging. Daarom moeten we opnieuw opmerken dat een reservoir van monomere soorten dat ze vrijgeeft als reactie op hun consumptie altijd nodig is om quasi-stationaire nucleatie in een gesloten systeem te bereiken. Alle klassieke theorieën over kiemvorming, inclusief de Becher-Döring-theorie, gaan impliciet uit van een dergelijke voorwaarde. Definitie van conductometrischanalysemethode werd gegeven in de secties van het bovenstaande artikel.
Andere wetenschappers hebben het proces van tijdelijke kiemvorming van zilverhalogenide onderzocht door gepulseerde radiolyse van water dat methyleenhalogenide en zilverionen bevat, waarbij het methyleenhalogenide wordt ontleed om halogenide-ionen vrij te maken door gehydrateerde elektronen die worden gegenereerd door gepulseerde straling in het bereik van 4 ns tot 3 μs. De spectra van de producten werden opgenomen met behulp van een fotomultiplier en streak-camera en er werden monomere zilverhalogenide-precursoren gevonden in de loop van een tijd in de orde van microseconden, gevolgd door een kiemvormingsproces vergelijkbaar met dat waargenomen door Tanaka en Iwasaki. Hun resultaten laten duidelijk zien dat het proces van kiemvorming van zilverhalogeniden door directe menging van de reactanten uit twee elementaire stappen bestaat; dat wil zeggen de vorming van een monomere voorloper in de orde van grootte van s en de daaropvolgende overgang naar kernen in de orde van grootte van 10 ms. Opgemerkt moet worden dat de gemiddelde grootte van kernen ongeveer 10 nm is.
Verzadiging
Wat betreft oververzadigingscoëfficiënten voor de kiemvorming van AgCl-deeltjes in open systemen waarin hoge concentraties reactanten zoals AgNO3 en KCl continu in de gelatine-oplossing worden geïntroduceerd tijdens de precipitatie, rapporteerden Strong en Wey31 1.029 (80 ° C) - 1.260 (40°C) en Leubner32 rapporteerden 1.024 bij 60°C zoals geschat op basis van het meten van de groeisnelheid van AgCl-zaaddeeltjes bij kritische oververzadiging. Dit is de essentie van de conductometrische methode van kwantitatieve analyse.
Aan de andere kant, voor open AgBr-deeltjessystemen, sommigegeschatte waarden van de kritische oververzadigingscoëfficiënt, Scrit: Scrit∼- 1,5 bij 70 °C volgens Wey en Strong33 uit de grootteafhankelijke maximale groeisnelheid bepaald door de renucleatiedrempel te vinden bij verschillende snelheden van het toevoegen van een AgNO3-oplossing aan een KBr oplossing in aanwezigheid van zaaddeeltjes door dubbele stralen; Scrit=1,2-1,5 bij 25°C volgens Jagannathan en Wey34 als de maximale oververzadigingsfactor bepaald met de Gibbs-Thomson-vergelijking met hun gegevens over de minimale gemiddelde grootte van kernen waargenomen door elektronenmicroscopie tijdens de kiemvormingsstap van AgBr-precipitatie met twee stralen. Dit is zeer effectief bij het toepassen van de conductometrische kwantificeringsmethode.

Bij het berekenen van deze Scrit-waarden namen ze γ=140 mJ m − 2. Aangezien nucleatie in open systemen overeenkomt met het overlevingsproces van ontluikende kernen die zijn gecreëerd in een lokale zone met extreem hoge oververzadiging nabij de reactantuitlaten, is kritiek oververzadiging komt overeen met de concentratie van de opgeloste stof in evenwicht met kernen van maximale grootte, als we de gegevens van Sugimoto35 gebruiken over de maximale straal van AgBr-kernen in open systemen (0,3 8,3 nm) met theoretische γ voor kubieke AgBr (=109 mJ m − 2) 3, dan wordt de kritische oververzadigingsfactor, Scrit, berekend als 1,36 bij 25°C (als wordt aangenomen dat γ 140 mJ/m2 is, dan is Scrit=1,48).
Dus in ieder geval kritische oververzadigingen inopen systemen van zilverhalogenidedeeltjes zijn typisch ruim onder de maximale oververzadigingen (waarschijnlijk dicht bij kritische oververzadigingen) in gesloten systemen. Dit komt omdat de gemiddelde straal van kernen gegenereerd in de lokale zone van een open systeem veel groter is dan rmin een gesloten systeem, waarschijnlijk door de onmiddellijke fusie van zeer geconcentreerde primaire kernen in de lokale zone van een open systeem met een hoge lokale elektrolytconcentratie.
Toepassing
Het gebruik van de conductometrische titratiemethode voor continue registratie tijdens enzymatische processen is uitgebreid bestudeerd en geanalyseerd. Bijna alle elektrochemische analysemethoden zijn gebaseerd op elektrochemische reacties (potentiometrie, voltammetrie, amperometrie, coulometrie).
De conductometrische analysemethode is een methode waarbij er ofwel helemaal geen elektrochemische reacties op de elektroden zijn, of er secundaire reacties zijn die verwaarloosd kunnen worden. Daarom is bij deze methode de belangrijkste eigenschap van de elektrolytoplossing in de grenslaag de elektrische geleidbaarheid, die varieert volgens een vrij groot aantal biologische reacties.
Voordelen
Conductometrische biosensoren hebben ook enkele voordelen ten opzichte van andere soorten transducers. Ten eerste kunnen ze worden gemaakt met behulp van goedkope standaard dunne-filmtechnologie. Dit, samen met het gebruik van een geoptimaliseerde methode voor het immobiliseren van biologisch materiaal, leidt tot een aanzienlijke verlaging van zowel de primaire kosten van apparaten alstotale analysekosten. Voor ingebouwde microbiosensoren is het eenvoudig om de differentiële meetmodus uit te voeren, die externe invloeden compenseert en de meetnauwkeurigheid aanzienlijk verbetert.
De gegevens laten duidelijk het grote potentieel van conductometrische biosensoren zien. Dit is echter nog steeds een vrij nieuwe trend in biosensoren, dus de ontwikkeling van commerciële apparaten heeft een veelbelovende toekomst.
Nieuwe methoden
Sommige wetenschappers hebben een algemene methode beschreven voor het meten van pKa door conductantie. Deze methode werd veel gebruikt tot ongeveer 1932 (voordat pH-meetmethoden werden gebruikt). De conductometrische methode is extreem temperatuurgevoelig en kan niet worden gebruikt om overlappende pKa-waarden te meten. Een mogelijk voordeel voor monsters zonder chromofoor is dat het kan worden gebruikt in zeer verdunde oplossingen, tot 2,8 × 10-5 M. De afgelopen jaren is conductometrie 87 gebruikt om de pKa van lidocaïne te meten, hoewel het verkregen resultaat 0,7 was per eenheid onder de algemeen aanvaarde pH-waarde.

Albert en Sergeant beschreven ook een methode voor het bepalen van pKa uit oplosbaarheidsmetingen. Zoals hierboven vermeld, is de oplosbaarheid afhankelijk van pKa, dus als de oplosbaarheid wordt gemeten bij meerdere pH-waarden op een curve, kan pKa worden bepaald. Peck en Benet beschreven een algemene methode voor het schatten van pKa-waarden voor monoprotische, diprotische en amfotere stoffen op basis van een reeks oplosbaarheids- en pH-metingen. Hansen en Hafliger verkregen de pKa van het monster, watontleedt snel door hydrolyse van zijn aanvankelijke oplossnelheden als functie van de pH in een roterende schijfinrichting. Het resultaat komt goed overeen met het pH/UV-resultaat, maar ontleding bemoeilijkt deze laatste methode. Dit is in grote lijnen een beschrijving van de conductometrische analysemethode.






