Corrosiesnelheid is een multifactoriële parameter die zowel afhangt van externe omgevingsomstandigheden als van de interne eigenschappen van het materiaal. In de normatieve en technische documentatie zijn er bepaalde beperkingen op de toegestane waarden van metaalvernietiging tijdens de werking van apparatuur en bouwconstructies om hun probleemloze werking te garanderen. In de techniek is er geen universele methode om de corrosiesnelheid te bepalen. Dit komt door de complexiteit van het in aanmerking nemen van alle factoren. De meest betrouwbare methode is om de bedrijfsgeschiedenis van de faciliteit te bestuderen.
Criteria

Momenteel worden verschillende corrosiesnelheden gebruikt in technisch ontwerp:
- Volgens de directe beoordelingsmethode: vermindering van de massa van een metalen onderdeel per oppervlakte-eenheid - gewichtsindicator (gemeten in gram per 1 m2 gedurende 1 uur); schadediepte (of doorlaatbaarheid corrosieproces), mm/jaar; de hoeveelheid vrijgekomen gasfase van corrosieproducten; de tijdsduur waarin de eerste corrosieschade optreedt; aantal corrosiecentra per oppervlakte-eenheidoppervlakken die in een bepaalde periode verschenen.
- Indirect geschat: stroomsterkte elektrochemische corrosie; elektrische weerstand; verandering in fysieke en mechanische kenmerken.
De eerste directe waarderingsindicator is de meest voorkomende.
Berekeningsformules
In het algemene geval wordt het gewichtsverlies dat de corrosiesnelheid van het metaal bepa alt, bepaald met de volgende formule:
Vkp=q/(St), waar q de afname van de massa van het metaal is, g;
S - oppervlakte van waaruit het materiaal is overgebracht, m2;
t - tijdsperiode, uren
Bepaal voor plaatwerk en daaruit gemaakte schalen de diepte-index (mm/jaar):
H=m/t, m is de penetratiediepte in het metaal.
Er is de volgende relatie tussen de eerste en tweede indicatoren die hierboven zijn beschreven:
H=8, 76Vkp/ρ, waar ρ de dichtheid van het materiaal is.
Belangrijkste factoren die de corrosiesnelheid beïnvloeden
De volgende groepen factoren beïnvloeden de snelheid van metaalvernietiging:
- intern, gerelateerd aan de fysische en chemische aard van het materiaal (fasestructuur, chemische samenstelling, oppervlakteruwheid van het onderdeel, rest- en bedrijfsspanningen in het materiaal, en andere);
- extern (omgevingsomstandigheden, bewegingssnelheid van een bijtend medium, temperatuur, samenstelling van de atmosfeer, aanwezigheid van remmers of stimulerende middelen, en andere);
- mechanisch (ontwikkeling van corrosiescheuren, vernietiging van metaal onder invloed van cyclische belastingen,cavitatie en fretting corrosie);
- ontwerpkenmerken (selectie van metaalkwaliteit, openingen tussen onderdelen, ruwheidsvereisten).
Fysische en chemische eigenschappen
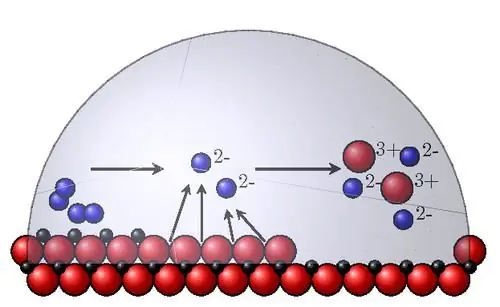
De belangrijkste interne corrosiefactoren zijn de volgende:
- Thermodynamische stabiliteit. Om het in waterige oplossingen te bepalen, worden referentie-Pourbaix-diagrammen gebruikt, langs de abscis waarvan de pH van het medium is uitgezet, en langs de ordinaat-as, de redoxpotentiaal. Een potentiële verschuiving in positieve richting betekent een grotere stabiliteit van het materiaal. Voorlopig wordt het gedefinieerd als de normale evenwichtspotentiaal van het metaal. In werkelijkheid corroderen materialen met verschillende snelheden.
- De positie van een atoom in het periodiek systeem van chemische elementen. De metalen die het meest vatbaar zijn voor corrosie zijn alkali- en aardalkalimetalen. De corrosiesnelheid neemt af naarmate het atoomnummer toeneemt.
- Kristalstructuur. Het heeft een dubbelzinnig effect op vernietiging. De grofkorrelige structuur zelf leidt niet tot een toename van corrosie, maar is gunstig voor de ontwikkeling van intergranulaire selectieve vernietiging van korrelgrenzen. Metalen en legeringen met een homogene verdeling van fasen corroderen gelijkmatig, terwijl die met een niet-uniforme verdeling corroderen volgens een focaal mechanisme. De onderlinge rangschikking van de fasen vervult de functie van anode en kathode in een agressieve omgeving.
- Energie-inhomogeniteit van atomen in het kristalrooster. Atomen met de hoogste energie bevinden zich op de hoeken van de gezichtenmicroruwheden en zijn actieve centra van ontbinding tijdens chemische corrosie. Daarom verhoogt zorgvuldige bewerking van metalen onderdelen (slijpen, polijsten, afwerken) de corrosieweerstand. Dit effect wordt ook verklaard door de vorming van dichtere en meer continue oxidefilms op gladde oppervlakken.
Invloed van gemiddelde zuurgraad

Tijdens het proces van chemische corrosie beïnvloedt de concentratie van waterstofionen de volgende punten:
- oplosbaarheid van corrosieproducten;
- vorming van beschermende oxidefilms;
- metaalvernietigingssnelheid.
Wanneer de pH in het bereik van 4-10 eenheden (zure oplossing) ligt, hangt de corrosie van ijzer af van de intensiteit van de zuurstofpenetratie naar het oppervlak van het object. In alkalische oplossingen neemt de corrosiesnelheid eerst af als gevolg van oppervlaktepassivering en neemt vervolgens, bij pH >13, toe als gevolg van het oplossen van de beschermende oxidefilm.
Voor elk type metaal is er zijn eigen afhankelijkheid van de intensiteit van vernietiging van de zuurgraad van de oplossing. Edelmetalen (Pt, Ag, Au) zijn bestand tegen corrosie in een zure omgeving. Zn, Al worden snel vernietigd in zowel zuren als alkaliën. Ni en Cd zijn bestand tegen alkaliën, maar corroderen gemakkelijk in zuren.
Samenstelling en concentratie van neutrale oplossingen

De mate van corrosie in neutrale oplossingen hangt meer af van de eigenschappen van het zout en de concentratie ervan:
- Tijdens de hydrolyse van zouten inin een corrosieve omgeving worden ionen gevormd die werken als activatoren of vertragers (remmers) van metaalvernietiging.
- De verbindingen die de pH verhogen, verhogen ook de snelheid van het destructieve proces (bijvoorbeeld natriumcarbonaat), en die welke de zuurgraad verlagen, verlagen deze (ammoniumchloride).
- In aanwezigheid van chloriden en sulfaten in de oplossing wordt de vernietiging geactiveerd totdat een bepaalde concentratie aan zouten is bereikt (wat wordt verklaard door de intensivering van het anodeproces onder invloed van chloride- en zwavelionen), en neemt vervolgens geleidelijk af als gevolg van een afname van de oplosbaarheid van zuurstof.
Sommige soorten zouten kunnen een onoplosbare film vormen (bijvoorbeeld ijzerfosfaat). Dit helpt het metaal te beschermen tegen verdere vernietiging. Deze eigenschap wordt gebruikt bij het aanbrengen van roestneutralisatoren.
Corrosieremmers
Corrosieremmers (of -remmers) verschillen in hun werkingsmechanisme op het redoxproces:
- Anode. Dankzij hen wordt een passieve film gevormd. Deze groep omvat verbindingen op basis van chromaten en bichromaten, nitraten en nitrieten. Het laatste type remmers wordt gebruikt voor interoperationele bescherming van onderdelen. Bij het gebruik van anodische corrosieremmers is het noodzakelijk om eerst hun minimale beschermende concentratie te bepalen, omdat toevoeging in kleine hoeveelheden kan leiden tot een toename van de vernietigingssnelheid.
- Kathode. Het werkingsmechanisme is gebaseerd op een afname van de zuurstofconcentratie en, dienovereenkomstig, een vertraging van het kathodische proces.
- Afscherming. Deze remmers isoleren het metaaloppervlak door onoplosbare verbindingen te vormen die als een beschermende laag worden afgezet.
De laatste groep omvat roestneutralisatoren, die ook worden gebruikt voor het reinigen van oxiden. Ze bevatten meestal fosforzuur. Onder zijn invloed treedt metaalfosfatering op - de vorming van een sterke beschermende laag van onoplosbare fosfaten. Neutralisatoren worden aangebracht met een spuitpistool of roller. Na 25-30 minuten krijgt het oppervlak een witgrijze kleur. Nadat de compositie is opgedroogd, worden verven en vernissen aangebracht.
Mechanische actie

Een toename van corrosie in een agressieve omgeving wordt mogelijk gemaakt door mechanische acties zoals:
- Interne (tijdens gieten of warmtebehandeling) en externe (onder invloed van een extern aangebrachte belasting) spanningen. Als gevolg hiervan treedt elektrochemische inhomogeniteit op, neemt de thermodynamische stabiliteit van het materiaal af en ontstaan corrosiescheuren. Vooral snel is de vernietiging onder trekbelastingen (scheuren worden gevormd in loodrechte vlakken) in aanwezigheid van oxiderende anionen, bijvoorbeeld NaCl. Een typisch voorbeeld van apparaten die onderhevig zijn aan dit soort vernietiging zijn onderdelen van stoomketels.
- Afwisselende dynamische actie, trillingen (corrosiemoeheid). Er is een intensieve verlaging van de vermoeiingsgrens, er ontstaan meerdere microscheurtjes, die vervolgens samensmelten tot één grote. Nummercycli tot falen hangt in grotere mate af van de chemische en fasesamenstelling van metalen en legeringen. Pompassen, veren, turbinebladen en andere apparatuur zijn onderhevig aan dergelijke corrosie.
- Wrijving van onderdelen. Snelle corrosie is te wijten aan mechanische slijtage van de beschermende films op het oppervlak van het onderdeel en chemische interactie met de omgeving. In vloeistof is de vernietigingssnelheid lager dan in lucht.
- Cavitatie-impact. Cavitatie treedt op wanneer de continuïteit van de vloeistofstroom wordt geschonden als gevolg van de vorming van vacuümbellen die instorten en een pulserend effect creëren. Hierdoor ontstaat er diepe schade van lokale aard. Dit type corrosie wordt vaak gezien in chemische apparaten.
Ontwerpfactoren

Bij het ontwerpen van elementen die in agressieve omstandigheden werken, moet er rekening mee worden gehouden dat de corrosiesnelheid toeneemt in de volgende gevallen:
- wanneer verschillende metalen met elkaar in contact komen (hoe groter het verschil in de elektrodepotentiaal ertussen, hoe hoger de stroomsterkte van het elektrochemische vernietigingsproces);
- in de aanwezigheid van mechanische spanningsconcentrators (groeven, groeven, gaten en andere);
- met een lage reinheid van het bewerkte oppervlak, omdat dit lokale kortgesloten galvanische paren tot gevolg heeft;
- met een significant verschil in temperatuur van afzonderlijke delen van het apparaat (er worden thermische galvanische cellen gevormd);
- in aanwezigheid van stilstaande zones (slots, gaten);
- bij het vormenrestspanningen, vooral in lasverbindingen (om ze te elimineren, is het noodzakelijk om te voorzien in warmtebehandeling - gloeien).
Evaluatiemethoden

Er zijn verschillende manieren om de mate van vernietiging van metalen in agressieve omgevingen te beoordelen:
- Laboratorium - monsters testen in kunstmatig gesimuleerde omstandigheden die bijna echt zijn. Hun voordeel is dat ze je in staat stellen de studietijd te verkorten.
- Field - gehouden in natuurlijke omstandigheden. Ze duren lang. Het voordeel van deze methode is het verkrijgen van informatie over de eigenschappen van het metaal in de omstandigheden van verdere bewerking.
- In-situ testen van afgewerkte metalen voorwerpen in de natuurlijke omgeving.






