Bij het bestuderen van het gedrag van gassen in de natuurkunde wordt veel aandacht besteed aan isoprocessen, dat wil zeggen, dergelijke overgangen tussen de toestanden van het systeem, waarbij één thermodynamische parameter behouden blijft. Er is echter een gasovergang tussen toestanden, die geen isoproces is, maar een belangrijke rol speelt in natuur en technologie. Dit is een adiabatisch proces. In dit artikel zullen we het in meer detail bekijken, met de nadruk op wat de gas adiabatische exponent is.
Adiabatisch proces
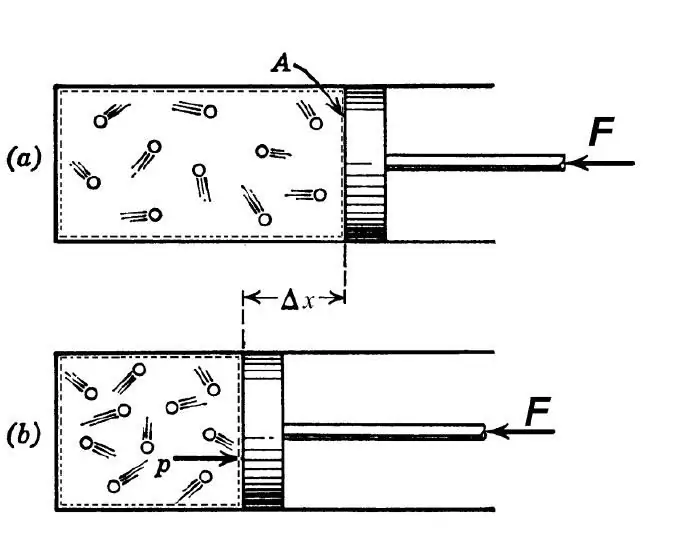
Volgens de thermodynamische definitie wordt onder een adiabatisch proces een dergelijke overgang verstaan tussen de begin- en eindtoestand van het systeem, waardoor er geen warmte-uitwisseling is tussen de externe omgeving en het bestudeerde systeem. Een dergelijk proces is mogelijk onder de volgende twee voorwaarden:
- thermische geleidbaarheid tussen de externe omgeving ensysteem is om de een of andere reden laag;
- de snelheid van het proces is hoog, dus de warmte-uitwisseling heeft geen tijd om op te treden.
In de techniek wordt de adiabatische overgang zowel gebruikt om het gas op te warmen tijdens zijn scherpe compressie als om het af te koelen tijdens snelle expansie. In de natuur manifesteert de betreffende thermodynamische overgang zich wanneer een luchtmassa stijgt of da alt van een helling. Dergelijke ups en downs leiden tot een verandering in het dauwpunt in de lucht en neerslag.
Poisson-vergelijking voor het adiabatische ideale gas

Een ideaal gas is een systeem waarin deeltjes willekeurig met hoge snelheden bewegen, geen interactie met elkaar hebben en dimensieloos zijn. Zo'n model is heel eenvoudig in termen van wiskundige beschrijving.
Volgens de definitie van een adiabatisch proces kan de volgende uitdrukking worden geschreven in overeenstemming met de eerste wet van de thermodynamica:
dU=-PdV.
Met andere woorden, een gas, dat uitzet of krimpt, werkt PdV vanwege een overeenkomstige verandering in zijn interne energie dU.
In het geval van een ideaal gas, als we de toestandsvergelijking gebruiken (wet van Clapeyron-Mendelejev), kunnen we de volgende uitdrukking krijgen:
PVγ=const.
Deze gelijkheid wordt de Poisson-vergelijking genoemd. Mensen die bekend zijn met gasfysica zullen opmerken dat als de waarde van γ gelijk is aan 1, de Poisson-vergelijking zal worden opgenomen in de wet van Boyle-Mariotte (isothermeVerwerken). Een dergelijke transformatie van de vergelijkingen is echter onmogelijk, aangezien γ voor elk type ideaal gas groter is dan één. De hoeveelheid γ (gamma) wordt de adiabatische index van een ideaal gas genoemd. Laten we de fysieke betekenis ervan nader bekijken.
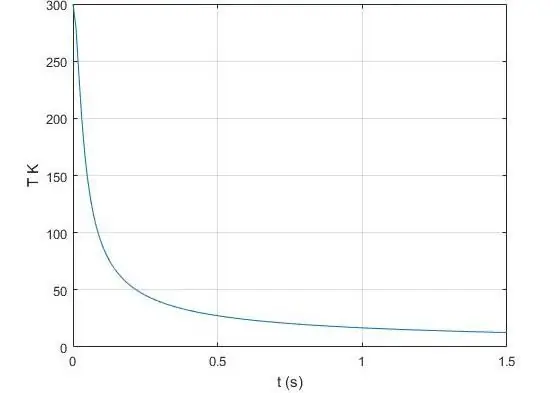
Wat is de adiabatische exponent?
De exponent γ, die voorkomt in de Poisson-vergelijking voor een ideaal gas, is de verhouding van de warmtecapaciteit bij constante druk tot dezelfde waarde, maar al bij constant volume. In de natuurkunde is warmtecapaciteit de hoeveelheid warmte die moet worden overgedragen aan of afgenomen van een bepaald systeem om de temperatuur met 1 Kelvin te veranderen. We zullen de isobare warmtecapaciteit aanduiden met het symbool CP, en de isochore warmtecapaciteit met het symbool CV. Dan geldt de gelijkheid voor γ:
γ=CP/CV.
Aangezien γ altijd groter is dan één, laat het zien hoe vaak de isobare warmtecapaciteit van het bestudeerde gassysteem de vergelijkbare isochoorkarakteristiek overschrijdt.
Warmtecapaciteiten van CP en CV
Om de adiabatische exponent te bepalen, moet men een goed begrip hebben van de betekenis van de grootheden CP en CV. Om dit te doen, zullen we het volgende gedachte-experiment uitvoeren: stel je voor dat het gas zich in een gesloten systeem in een vat met massieve wanden bevindt. Als het vat wordt verwarmd, wordt idealiter alle gecommuniceerde warmte omgezet in de interne energie van het gas. In een dergelijke situatie is gelijkheid geldig:
dU=CVdT.
WaardeCVdefinieert de hoeveelheid warmte die moet worden overgedragen aan het systeem om het isochorisch te verwarmen met 1 K.
Stel nu dat het gas zich in een vat met een bewegende zuiger bevindt. Tijdens het verwarmen van een dergelijk systeem zal de zuiger bewegen, waardoor een constante druk wordt gehandhaafd. Aangezien de enthalpie van het systeem in dit geval gelijk zal zijn aan het product van de isobare warmtecapaciteit en de verandering in temperatuur, zal de eerste wet van de thermodynamica de vorm aannemen:
CPdT=CVdT + PdV.
Vanaf hier is te zien dat CP>CV, aangezien het in het geval van een isobare toestandsverandering nodig is om niet alleen warmte gebruiken om de temperatuur van het systeem te verhogen, en dus de interne energie, maar ook het werk dat het gas doet tijdens zijn expansie.
De waarde van γ voor een ideaal eenatomig gas
Het eenvoudigste gassysteem is een monoatomisch ideaal gas. Stel we hebben 1 mol van zo'n gas. Bedenk dat in het proces van isobare verwarming van 1 mol gas met slechts 1 Kelvin, het werkt gelijk aan R. Dit symbool wordt gewoonlijk gebruikt om de universele gasconstante aan te duiden. Het is gelijk aan 8, 314 J / (molK). Als we de laatste uitdrukking in de vorige paragraaf voor dit geval toepassen, krijgen we de volgende gelijkheid:
CP=CV+ R.
Van waaruit u de waarde van isochore warmtecapaciteit kunt bepalen CV:
γ=CP/CV;
CV=R/(γ-1).
Het is bekend dat voor één molmonoatomisch gas, de waarde van de isochore warmtecapaciteit is:
CV=3/2R.
Van de laatste twee gelijkheden volgt de waarde van de adiabatische exponent:
3/2R=R/(γ-1)=>
γ=5/3 ≈ 1, 67.
Merk op dat de waarde van γ uitsluitend afhangt van de interne eigenschappen van het gas zelf (van de polyatomaire aard van zijn moleculen) en niet afhangt van de hoeveelheid stof in het systeem.
Afhankelijkheid van γ van het aantal vrijheidsgraden
De vergelijking voor de isochore warmtecapaciteit van een monoatomisch gas is hierboven geschreven. De coëfficiënt 3/2 die erin voorkwam is gerelateerd aan het aantal vrijheidsgraden in één atoom. Het kan alleen in een van de drie richtingen van de ruimte bewegen, dat wil zeggen dat er alleen translationele vrijheidsgraden zijn.
Als het systeem wordt gevormd door diatomische moleculen, worden er nog twee rotatiegraden toegevoegd aan de drie translatiegraden. Daarom wordt de uitdrukking voor CV:
CV=5/2R.
Dan is de waarde van γ:
γ=7/5=1, 4.
Merk op dat het diatomische molecuul eigenlijk nog één trillingsvrijheidsgraad heeft, maar bij temperaturen van enkele honderden Kelvin wordt het niet geactiveerd en draagt het niet bij aan de warmtecapaciteit.
Als gasmoleculen uit meer dan twee atomen bestaan, hebben ze 6 vrijheidsgraden. De adiabatische exponent is in dit geval gelijk aan:
γ=4/3 ≈ 1, 33.
SoDus als het aantal atomen in een gasmolecuul toeneemt, neemt de waarde van γ af. Als je een adiabatische grafiek bouwt in de P-V-assen, zul je merken dat de curve voor een monoatomisch gas zich scherper zal gedragen dan voor een polyatomaire.
Adiabatische exponent voor een mengsel van gassen
We hebben hierboven laten zien dat de waarde van γ niet afhangt van de chemische samenstelling van het gassysteem. Het hangt echter af van het aantal atomen waaruit de moleculen bestaan. Laten we aannemen dat het systeem uit N componenten bestaat. De atoomfractie van component i in het mengsel is ai. Om vervolgens de adiabatische exponent van het mengsel te bepalen, kunt u de volgende uitdrukking gebruiken:
γ=∑i=1N(aiγ i).
Waar γi de γ-waarde is voor de i-de component.
Deze uitdrukking kan bijvoorbeeld worden gebruikt om de γ van lucht te bepalen. Aangezien het voor 99% uit diatomische moleculen van zuurstof en stikstof bestaat, moet de adiabatische index zeer dicht bij de waarde van 1,4 liggen, wat wordt bevestigd door de experimentele bepaling van deze waarde.






