Kennis van definities in de natuurkunde is een sleutelfactor voor het succesvol oplossen van verschillende fysieke problemen. In het artikel zullen we bekijken wat wordt bedoeld met isobare, isochoor, isotherme en adiabatische processen voor een ideaal gassysteem.
Ideaal gas en zijn vergelijking
Laten we, voordat we verder gaan met de beschrijving van isobare, isochore en isotherme processen, eens kijken wat een ideaal gas is. Onder deze definitie in de natuurkunde beschouwen ze een systeem dat bestaat uit een enorm aantal dimensieloze en niet-interagerende deeltjes die met hoge snelheden in alle richtingen bewegen. In feite hebben we het over een gasvormige geaggregeerde toestand van materie, waarin de afstanden tussen atomen en moleculen hun afmetingen ver overschrijden en waarin de potentiële energie van interactie van deeltjes wordt verwaarloosd vanwege de kleinheid ervan, vergeleken met de kinetische energie.
De toestand van een ideaal gas is het geheel van zijn thermodynamische parameters. De belangrijkste zijn temperatuur, volume en druk. Laten we ze respectievelijk aanduiden met de letters T, V en P. In de jaren '30 van de 19e eeuwClapeyron (een Franse wetenschapper) schreef eerst een vergelijking op die de aangegeven thermodynamische parameters combineert binnen een enkele gelijkheid. Het ziet eruit als:
PV=nRT,
waarbij n en R respectievelijk de hoeveelheid stoffen en de gasconstante zijn.
Wat zijn isoprocessen in gassen?
Zoals velen hebben opgemerkt, gebruiken isobare, isochore en isotherme processen hetzelfde "iso"-voorvoegsel in hun naam. Het betekent de gelijkheid van één thermodynamische parameter tijdens het doorlopen van het hele proces, terwijl de overige parameters veranderen. Een isotherm proces geeft bijvoorbeeld aan dat daardoor de absolute temperatuur van het systeem constant wordt gehouden, terwijl een isochoor proces een constant volume aangeeft.
Isoprocessen zijn gemakkelijk te bestuderen, omdat het vastleggen van een van de thermodynamische parameters leidt tot een vereenvoudiging van de algemene vergelijking van de gastoestand. Het is belangrijk op te merken dat de gaswetten voor al deze isoprocessen experimenteel zijn ontdekt. Hun analyse stelde Clapeyron in staat om de gereduceerde universele vergelijking te verkrijgen.
Isobare, isochore en isotherme processen
De eerste wet werd ontdekt voor een isotherm proces in een ideaal gas. Nu heet het de wet van Boyle-Mariotte. Aangezien T niet verandert, impliceert de toestandsvergelijking de gelijkheid:
PV=const.
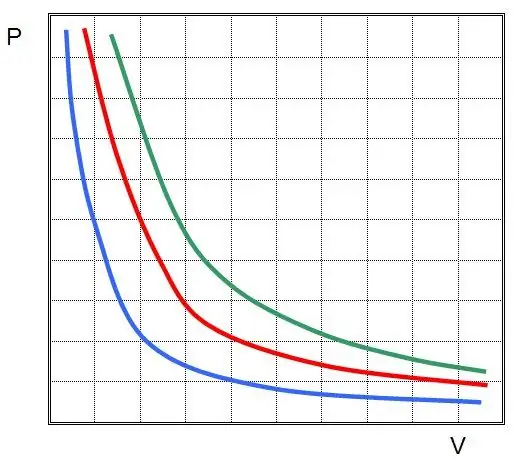
Met andere woorden, elke verandering in druk in het systeem leidt tot een omgekeerd evenredige verandering in het volume, als de temperatuur van het gas constant wordt gehouden. De grafiek van de functie P(V) ishyperbool.
Isobaar proces - dit is een verandering in de toestand van het systeem, waarbij de druk constant blijft. Nadat we de waarde van P in de Clapeyron-vergelijking hebben vastgelegd, krijgen we de volgende wet:
V/T=const.
Deze gelijkheid draagt de naam van de Franse natuurkundige Jacques Charles, die hem aan het einde van de 18e eeuw ontving. De isobar (grafische weergave van de V(T)-functie) ziet eruit als een rechte lijn. Hoe meer druk in het systeem, hoe sneller deze lijn stijgt.
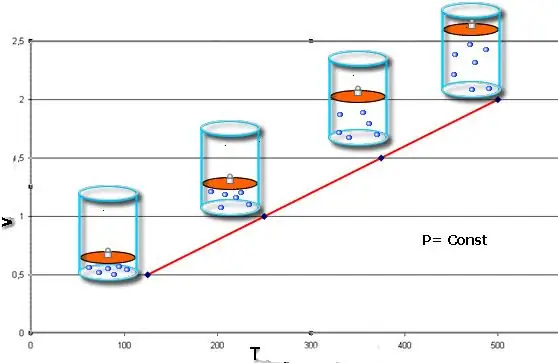
Het isobare proces is eenvoudig te implementeren als het gas onder de zuiger wordt verwarmd. De moleculen van deze laatste verhogen hun snelheid (kinetische energie), creëren een hogere druk op de zuiger, wat leidt tot de expansie van het gas en het handhaven van een constante waarde van P.
Ten slotte is het derde isoproces isochoor. Hij draait met een constant volume. Uit de toestandsvergelijking verkrijgen we de overeenkomstige gelijkheid:
P/T=const.
Het staat onder natuurkundigen bekend als de wet van Gay-Lussac. De directe evenredigheid tussen druk en absolute temperatuur geeft aan dat de grafiek van het isochore proces, net als de grafiek van het isobare, een rechte lijn is met een positieve helling.
Het is belangrijk om te begrijpen dat alle isoprocessen voorkomen in gesloten systemen, dat wil zeggen dat de waarde van n behouden blijft tijdens hun verloop.
Adiabatisch proces
Dit proces behoort niet tot de categorie "iso", aangezien alle drie de thermodynamische parameters tijdens de passage veranderen. adiabatischde overgang genoemd tussen twee toestanden van het systeem, waarin het geen warmte uitwisselt met de omgeving. De uitbreiding van het systeem wordt dus uitgevoerd vanwege de interne energiereserves, wat leidt tot een aanzienlijke daling van de druk en absolute temperatuur erin.
Adiabatisch proces voor een ideaal gas wordt beschreven door de vergelijkingen van Poisson. Een van hen wordt hieronder getoond:
PVγ=const,
waar γ de verhouding is van warmtecapaciteiten bij constante druk en bij constant volume.
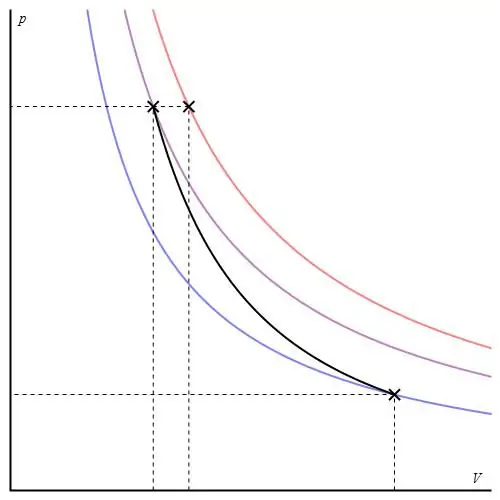
De adiabatische grafiek verschilt van de isochore procesgrafiek en van de isobare grafiek, maar is vergelijkbaar met een hyperbool (isotherm). De adiabat in de P-V-assen gedraagt zich scherper dan de isotherm.






